Introduzione
L’importanza biologica e medica della variazione genomica, responsabile della suscettibilità a diverse malattie comuni o della risposta ai farmaci, ha stimolato lo sviluppo di nuovi metodi diagnostici per l’analisi genetica. L’analisi del DNA genomico richiede fasi preliminari come l’estrazione e la purificazione degli acidi nucleici target, seguite da amplificazione, sequenziamento e rilevamento. Questi processi, laboriosi e dispendiosi in termini di tempo, comportano spesso costi elevati e possono compromettere l’accuratezza diagnostica a causa di possibili contaminazioni durante le manipolazioni manuali.
Parallelamente, i progressi nella tecnologia microfluidica hanno permesso lo sviluppo di sistemi miniaturizzati impiegati in numerose applicazioni biomediche, inclusa la diagnosi rapida di malattie genetiche. Questi sistemi innovativi aumentano significativamente la sensibilità diagnostica dei metodi di rilevamento del DNA, riducendo al contempo il consumo di campioni e reagenti, migliorando la produttività e abbattendo tempi e costi di analisi. In particolare, la tecnologia a goccia microfluidica è vantaggiosa quando è richiesta l’analisi a livello di singola cellula o singola molecola, fondamentale per comprendere gli effetti dell’eterogeneità nelle popolazioni cellulari.
Gli esperimenti sono stati condotti su linee cellulari ben caratterizzate fornite dall’American Type Culture Collection (ATCC) e coltivate secondo i protocolli ATCC. Per le analisi su EBV, sono state utilizzate le linee BC-1 (CRL-2230) e CESS (TIB-190), entrambe cellule B positive per EBV, mentre come controlli sono state impiegate le linee EBV-negative Ramos (CRL-1596) e CCRF-CEM (CCL-119).
I siti target per la formazione dei PD-loop sono stati selezionati nel genoma di Human Herpesvirus 4 (EBV) disponibile nel Genomes Database. I PNAs sono stati acquistati da Panagene Inc. e progettati per legarsi a sequenze specifiche di 20–30 bp, con tratti omopurina–omopirimidina di 7–10 bp come siti di apertura. Le sonde padlock sono complementari al filamento DNA sostituito, permettendo la circolarizzazione e il collegamento topologico al DNA target. Tutte le sonde oligonucleotidiche sono state acquistate da Integrated DNA Technologies.
Circa 10^6 cellule sono state fissate in formaldeide al 4% e trattate con PNAs a 45°C per 4 h. La circolarizzazione delle sonde padlock è stata effettuata con T4 DNA ligasi a 37°C per 2 h. La reazione di amplificazione tramite RCA è stata eseguita con phi29 DNA polimerasi, primer, dNTP e sonde fluorescenti per 2 h a 37°C. Le cellule sono state analizzate mediante citometria a flusso (BD FACSCalibur™) e osservate al microscopio fluorescente dopo colorazione con DAPI.
Le camere microfluidiche sono state realizzate mediante litografia morbida con SU-8 su wafer di silicio, PDMS colato, reticolato e legato a vetrini attivati al plasma. I canali sono stati trattati con Aquapel e connessi a siringhe tramite tubi di polietilene; le pompe a siringa hanno controllato i flussi di cellule, reagenti e fase olio.
Le gocce sono state formate nella zona di flow-focusing, con flusso centrale contenente cellule (10^5/ml) e mix RCA, e flussi laterali di olio con surfattante. Il rapporto flussi acqua/olio è stato regolato per ottenere gocce di ≈1,8 nl (diametro ≈150 µm).
Le immagini fluorescenti delle gocce sono state acquisite con microscopio Zeiss 200 Axiovert e telecamera digitale AxioCAM MRm. I segnali fluorescenti sono stati separati per Cy3 e analizzati con ImageJ per quantificare la presenza di DNA virale e l’efficacia della reazione RCA.
Materiali e Metodi
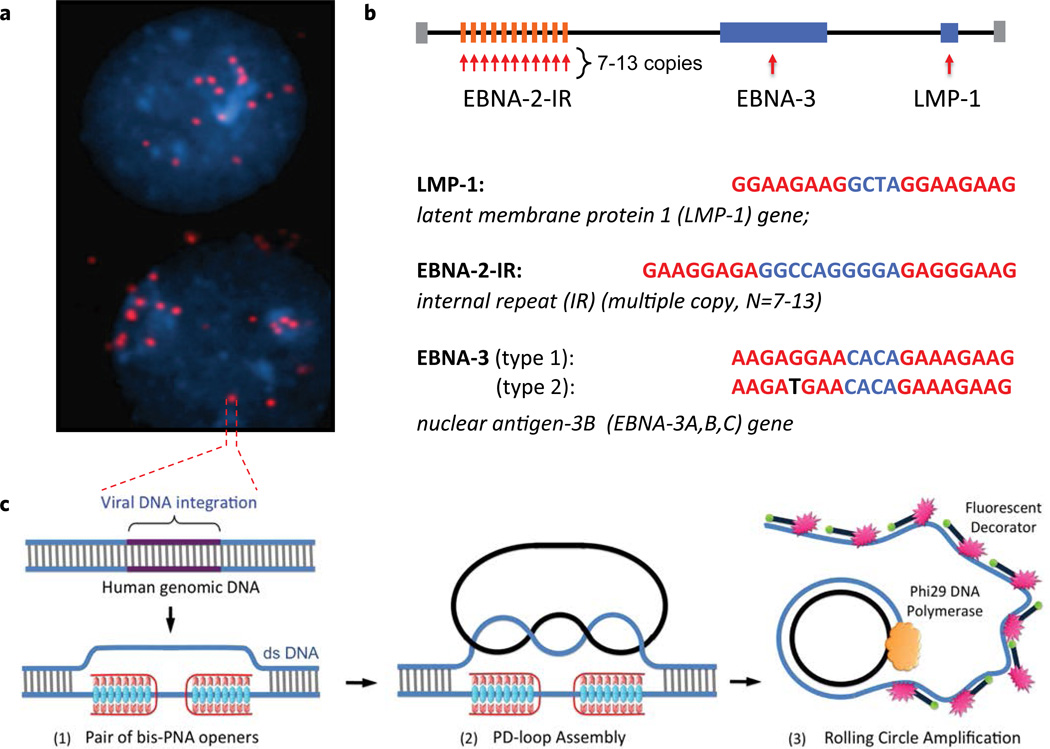
Per validare il metodo, sono stati condotti esperimenti sulla linea cellulare umana BC-1, nota per essere EBV-positiva, mentre la linea CCRF-CEM, priva di EBV, è stata utilizzata come controllo negativo. Sono stati selezionati tre siti caratteristici del virus Epstein–Barr: LMP1, associato alla proteina trasformante principale del virus; EBNA-3, coinvolto nella regolazione dell’espressione genica virale; ed EBNA-2IR, una regione ripetuta multipla presente nel gene dell’antigene nucleare della fase latente.
Il DNA delle cellule fissate è stato trattato con sonde bis-PNA, seguito dall’ibridazione con una padlock probe e dall’amplificazione tramite Rolling Circle Amplification (RCA). L’osservazione mediante microscopia a fluorescenza ha rivelato numerosi segnali fluorescenti nei nuclei delle cellule BC-1, confermando che il virus EBV può essere presente in circa 2–30 copie per cellula.
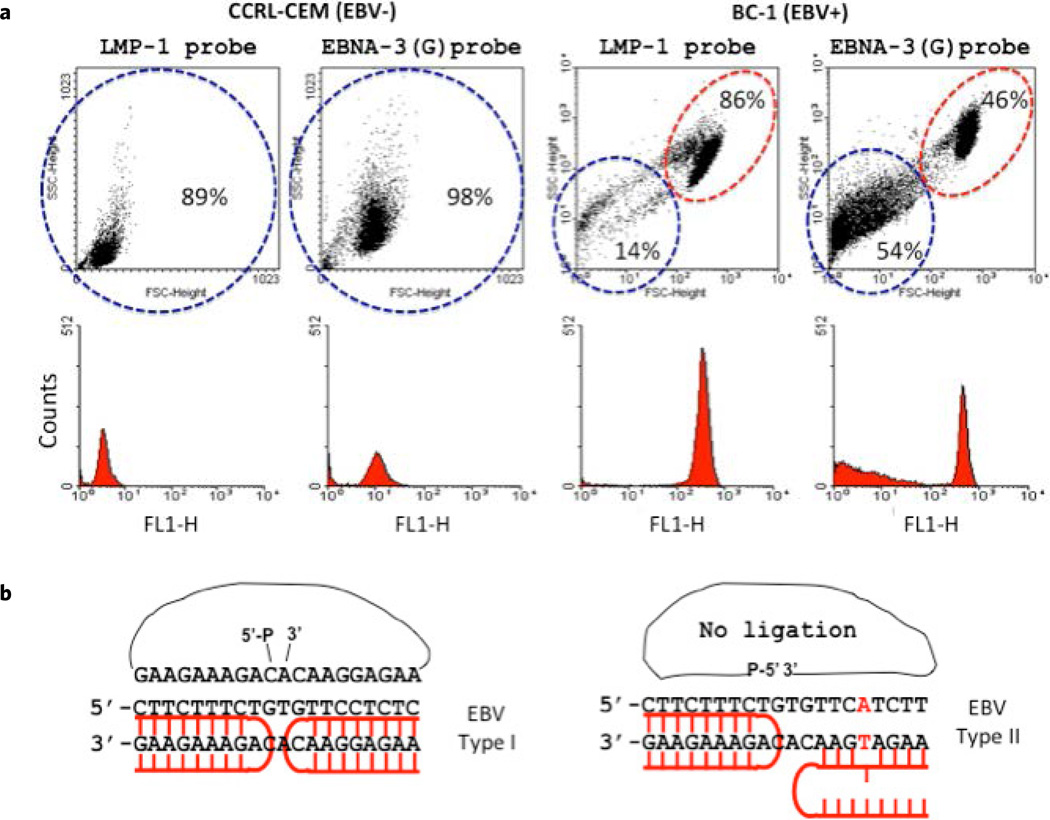
Successivamente, la procedura è stata applicata in un sistema cells-in-flow utilizzando sia cellule BC-1 (EBV+) che CCRF-CEM (EBV−). Le cellule BC-1 hanno mostrato un segnale fluorescente significativamente più elevato rispetto al controllo negativo. Ulteriori controlli senza sonde PNA o con sonde PNA non specifiche hanno prodotto solo segnali di fondo, dimostrando che il sistema PNA-RCA in flusso consente una rilevazione specifica e affidabile dell’EBV.